Kemijske veze
Međuatomske veze
-
ionska, kovalentna i metalna
-
kemijske veze među atomima elemenata nastaju zbog težnje ka smanjenju energije sustava
-
većina atoma elemenata nema popunjenu zadnju ljusku elektronskog omotača, pa želi postići oktet zadnje ljuske (ili dublet kod vodika i helija)
Ionska veza
-
ionska veza nastaje između atoma metala i nemetala
-
pri tome metal gubi elektrone i postaje kation, a nemetal prima elektrone i postaje anion
-
ionska veza je elektrostatske prirode
-
zbog jakih privlačnih sila među ionima ionski kristali su tvrdi te imaju visoka tališta i vrelišta
-
ionski su spojevi dobro topljivi u vodi jer imaju polaran karakter
-
ionska veza je jača što je razlika elektronegativnosti elemenata veća, a isto tako ionska je veza jača što je veći nabojni broj iona
Kovalentna veza
-
zbog relativno male razlike elektronegativnosti među atomima nemetala, ne može doći do prijelaza elektrona s jednog atoma na drugi.
-
atomi nemetala tvore jedan ili više zajedničkih (veznih ili podijeljenih) elektronskih parova
-
to je kovalentna veza koja se predočuje crticom između spojenih atoma, a odnosi se na jedan vezni elektronski par
-
ovisno o broju zajedničkih elektronskih parova koji povezuju atome razlikujemo jednostruku, dvostruku i trostruku kovaletnu vezu
-
tvari nastale kovalentnom vezom sastoje se od molekula koje imaju određenu strukturu i geometrijski oblik te određeno usmjerenje u prostoru
-
kutovi među vezama ovise o broju atoma u molekuli te broju veznih i neveznih elektronskih parova oko središnjeg atoma
-
međusobno se odbijaju nevezni elektronski parovi, nevezni i vezni, te vezni parovi međusobno
-
molekule tvari s kovalentnom vezom međusobno su slabo povezane i mogu se lako odijeliti
-
takve su tvari često plinovi i tekućine
-
ako su u krutom agregacijskom stanju, onda lako sublimiraju, mekane su i imaju nisko talište i vrelište
-
nepolarne molekule s kovalentnom vezom nisu topljive u vodi, dok molekule koje su polarnog karaktera jesu topljive u vodi
Duljina kovalentne veze je udaljenost među jezgara vezanih kovalentnom vezom
Kovalentni polumjer atoma je polovica razmaka dvaju istovrsnih atoma vezanih kovalentnom vezom
Van der Waalsov polumjer je polovina udaljenosti između jezgara dvaju istovrsnih atoma koji su u dodiru, ali nisu u kemijskoj vezi
Donorsko (koordinativna) kovalentna veza
-
kovalentna veza kod koje zajednički elektronski par potječe od samo jednog atoma
-
primjeri molekula u kojima postoji osim običnih kovalentnih veza i donorska kovalentna veza: ozon, ugljikov monoksid, dušikov(V)oksid, nitratna kiselina, sulfatna kiselina….
Polarnost kovalentne veze
-
ako su atomi u molekuli iste elektronegativnosti podjela zajedničkog elektronskog para je ravnopravna te će molekula biti nepolarna
-
ako su atomi u molekuli različite elektronegativnosti, zajednički elektronski par privlači se više jezgri elektronegativnijeg elementa pa je molekula polarna
-
polarne molekule imaju dva pola, razdvojeno težište pozitivnog i negativnog pola
-
polarnost molekule uzrokuju dva efekta: razlika u elektronegativnosti atoma u vezi i prostorna građa molekule
Odstupanje od pravila okteta
Ukoliko centralni atom u molekuli nema oko sebe osam elektrona, kaže se da postoji odstupanje od pravila okteta. Primjer: berilijev klorid, BeCl2, borov trifluorid, BF3, fosforov(V)klorid, PCl5, sumporov(VI)fluorid, SF6.
Metalna veza
Ostvaruje se između atoma metala. U kristalnoj rešetki metala dolazi do preklapanja atomskih orbitala jer su bliske po energiji i stvaraju se molekulske orbitale. Tako se iz pojedinih vrsta atomskih orbitala stvaraju elektronske vrpce (zone). U kristalnoj rešetki metala ima više energijskih nivoa nego što ima elektrona elektrona da ih popune.
Valentna vrpca
-
energetski nivoi koji su popunjeni elektronima.
Vodljiva vrpca
-
prazni energetski nivoi
-
oni omogućuju elektronima da pod utjecajem vanjskog električnog polja poprime veći sadržaj energije i da putuju kroz kristal, pa metal provodi električnu struju
-
u metalima su valentna i vodljiva vrpca tako blizu (preklapaju se) da elektroni bez zapreke prelaze iz jedne u drugu., (vodiči)
Poluvodiči
-
tvari u kojima između valentne i vodljive vrpce postoji određena energetska barijera koju elektroni moraju svladati da bi prešli iz jedne u drugu (električna vodljivost takve tvari se smanjuje)
Izolatori
-
tvari koje ne provode električnu struju jer je energetska barijera između valentne i vodljive vrpce toliko velika da je eletroni ne mogu svladati
Međumolekulske veze: vodikova veza i van der Waalsove sile
Vodikova veza
-
elektrostatske prirode
-
nešto jača od van der Waalsovih sila, ali slabija od međuatomskih veza
-
spojevi među čijim molekulama postoje vodikove veze imaju mnogo viša tališta i vrelišta od očekivanih vrijednosti jer su i privlačne sile među molekulama jače
-
u sastavu molekule mora biti vodik i izazito elektronegativan element(npr; F, O, N),
-
molekula mora biti polarne građe
Van der Waalsove sile
-
slabije od međuatomskih veza
-
ovisi o veličini čestica (što su čestice veće, to je među njima više dodira pa su i privlačne sile jače)
-
o jakosti ovih sila ovise tališta i vrelišta tvari pa i agregacijsko stanje tvari – vrelišta rastu porastom relativnih atomskih masa, odnosno porastom veličine atoma i molekula
Kristali: ionski, molekulski i atomski ( kristali metala i nemetala)
1. Ionski kristali:
Karakteristična svojstva ionskih spojeva:
-
polimorfija
-
velika tvrdoća
-
kalavost
-
koordinacijski broj
-
taljevine i vodene otopine provode el. struju
-
dobra topljivost u vodi
-
relativno visoko talište i vrelište:
-
veći naboj iona – veće privlačne sile
-
manji razmak iona – veće privlačne sile
2. Molekulski kristali:
Karakteristična svojstva molekulskih kristala:
-
relativno mekani
-
nisko talište i vrelište
-
uglavnom netopljivi u vodi
-
dobro topljivi u organskim otapalima
-
ne provode el. struju
3. Atomski kristali (kovalentni):
-
dijamant: visoko talište, velika tvrdoća i izolator
-
grafit: visoko talište, mekan i vodič
4. Kristali metala:
-
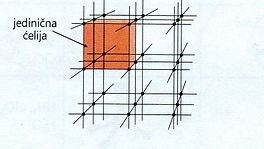
Kristalna rešetka – razmještaj čestica od kojeg je izgrađen kristal
-
Jedinična elementarna ćelija – najmanji dio kristalne rešetke koji se ponavlja u prostoru
-
Prostorno centrirana kubična slagalina: 8 x 1/8 + 1 = 2
-
Plošno centrirana kubična slagalina: 8 x 1/8 + 6 x ½ = 4
-
visoka tališta i vrelišta
-
velika gustoća i tvrdoća
-
vodiči električne struje